Autor : Da Lozzo Alejandro G1, Jorro BarĂłn Facundo A.2, GarcĂa MartĂ Sebastián3
1 - 2Maestrando en MaestrĂa en efectividad clĂnica, FMED, UBA 3Coord. de evaluaciĂłn de tecnologĂas sanitarias y economĂa de la salud, Instituto de efectividad clĂnica y sanitaria
Correspondencia : Alejandro Da Lozzo e-mail: alejandro.dalozzo@hospitalitaliano.org.ar
Resumen
Introducción: La injuria pulmonar aguda (IPA) se asocia con altas tasas de mortalidad. El tratamiento se basa principalmente en la ventilación mecánica (VM), con distintas variantes. Los dispositivos de soporte pulmonar extracorpóreo (ECLS) pueden proporcionar suficiente intercambio gaseoso en pacientes con IPA, cuando a pesar de la optimización del tratamiento habitual persiste hipoxemia o hipercapnia con acidosis respiratoria grave. Los dispositivos pueden ser con bomba (ECMO) o sin bomba (pECLA). El uso de ECMO y pECLA están autorizados en Argentina, Reino Unido (RU) y EEUU, y en la mayoría de los países europeos.
Objetivo: Evaluar si disminuye la mortalidad con el uso de dispositivos de ECLS asociados a VM contra el uso de VM solamente, en pacientes adultos con IPA aguda grave. Secundariamente, se evaluará en dichos grupos los días libres de VM al día 28, los días de estancia hospitalaria, los días de estancia en UCI, las diferencias a nivel hemodinámico y respiratorio del ECMOvv y los pECLA. Finalmente se evaluarán reportes de costo-efectividad.
Método: Se efectuó una revisión sistemática en TripDataBase, Pubmed, buscadores genéricos y sitios específicos. Se buscaron políticas de cobertura.
Resultados: Se hallaron 4 ECCA, 8 SC, 4 estudios secundarios, 2 evaluaciones económicas y 1 ETS. Además, se localizaron políticas de cobertura en el RU y EEUU.
Conclusiones: Se evidencia reducción de mortalidad en el corto tiempo (30 días o intrahospitalaria) en comparación con VM. No se encontraron diferencias a largo plazo, en días libres de VM-28d, en estancia hospitalaria, ni en UCI. En pECLA la evidencia es de menor calidad y no hay evidencia de reducción de mortalidad. Los parámetros hemodinámicos no son modificados por el ECMOvv, ni por pECLA. ECMOav es útil en casos de inestabilidad hemodinámica. La transferencia de gas pulmonar mejora con el uso de ECLS (reducción de PaCO2 y aumento de PaO2). El mayor beneficio se encuentra en el tratamiento de la hipercapnia, para la cual pECLA parecen ser los más indicados, en relación a su menor complejidad y costo. Muchas publicaciones coinciden en tasas menores de complicaciones con pECLA vs ECMOvv, en particular con respecto a la coagulación y hemólisis. Las indicaciones deben ser estrictamente controladas y monitorizadas. Los sistemas de salud hacen especial hincapié en la derivación a centros de alto volumen y complejidad para su uso. Encontramos costo efectividad para ECMO en los sistemas de salud de EEUU y RU, con valores de USD 7.000-35.000 por año de vida o QALY ganado y de £19.252 (IC95% 7.622-59.200) para pECLA.
Palabras clave: Dispositivos extracorpóreos; Soporto pulmonar; Insuficiencia pulmonar severa.
Abstract
Evaluation of extracorporeal lung support devices in adults with severe acute lung failure
Introduction: Acute lung injury (ALI) is associated with high mortality rates. Treatment is based on mechanical ventilation (MV). Extracorporeal lung support (ECLS) devices can provide sufficient gas exchange in patients with ALI when hypoxemia or hypercapnia persists with severe respiratory acidosis despite usual treatment. A pump can be used (ExtraCorporeal Membrane Oxigenator - ECMO) or not (pumpless ExtraCorporeal Lung Support - pECLA) towards to move blood stream in these devices. ECMO and pECLA are authorized in Argentina, UK, USA and most European countries.
Objective: To evaluate decreasement in mortality with ECLS+MV vs. MV alone in adult patients with severe ALI. To evaluate MV-free-28-days, hospital length of stay (LOS), ICU LOS, differences in hemodynamic and respiratory parameters in vvECMO vs. pECLA. Cost-effectiveness will be evaluated.
Methods: A systematic review in Tripdatabase, Pubmed, general search engines and specific sites was made. Coverage policies were sought.
Results: 4 randomized controlled trials, 8 case series, 4 secondary studies, 2 economic evaluations and 1 sanitary technology evaluation were found. UK and USA coverage policies were located.
Conclusions: ECLS+VM demonstrated reduction in 30-days-mortality compared to VM alone. No other differences (MV-free-28-days, LOS, ICU LOS) were found. Evidence about use of pECLA is low quality. There is no evidence in mortality reduction with pECLA. Hemodynamic parameters are not modified by vvECMO nor pECLA. avECMO is useful in hemodynamic instability. ECLS enhances lung gas transfer (CO2 arterial pressure reduction and O2 arterial pressure increase). More important benefits are achieved in hypercapnia treatment where pECLA seem to be more suitable because of its lower complexity and cost. There is lower complication rates in pECLA vs. vvECMO, particularly respect to coagulation and hemolysis complications. Indications should be strictly controlled and monitored. There is high recommendation on referral to high-volume centers for use of ECLS. ECMO is cost effective in US and UK health systems with USD 7,000-35,000 per life year or QALY gained and £ 19,252 (95% CI 7622-59200) for pECLA.
Abreviaturas utilizadas
ECCA: Ensayo Clínico Controlado y Aleatorizado
ECCO2R: dispositivos extracorpóreos de remoción de CO2
ECLS: ExtraCorporeal Lung Support (Soporte Pulmonar Extra Corpóreo)
ECMO: ExtraCorporeal Membrane Oxygenation (Membrana de Oxigenación Extracorpórea)
ECMOav: ECMO arterio-venoso
ECMOvv: ECMO veno-venoso
EEUU: Estados Unidos de Norteamérica
ETS: Evaluación de Tecnologías Sanitarias
FC: frecuencia cardíaca
FiO2: fracción inspirada de oxígeno
GC: gasto cardíaco
GPC: guías de práctica clínica
IMC: índice de masa corporal
• IPA: injuria pulmonar aguda
• PaCO2: presión arterial de dióxido de carbono
• PaO2: presión arterial de oxígeno
• pECLA: Pumpless ExtraCorporeal Lung Assist (Asistencia Pulmonar Extracorpórea Sin Bomba)
• RR: riesgo relativo
• RS: revisiones sistemáticas
• RU: Reino Unido
• SC: Serie de casos
• SDRA: síndrome de dificultad respiratoria del adulto
• TAM: presión arterial media
• UCI: Unidad de Cuidados Intensivos
• VM: ventilación mecánica
Introducción
La injuria pulmonar aguda (IPA) se asocia con tasas de mortalidad que oscilan entre un 30% y 40%, independientemente del tratamiento instaurado1. La principal causa es el síndrome de dificultad respiratoria del adulto (SDRA), que se caracteriza por insuficiencia respiratoria con severa hipoxemia y/o hipercapnia. La definición2 (de Berlín) de SDRA toma cuatro componentes para el diagnóstico: tiempo, radiografía de tórax, origen del edema y alteración de la oxigenación (Cuadro 1).

El tratamiento se basa principalmente en la ventilación mecánica (VM), incluyendo la estrategia de ventilación con bajos volúmenes pulmonares y la optimización de la presión positiva al final de la espiración (PEEP, Positive End Expiratory Pressure), respiración espontánea y la posición prona. El uso de óxido nítrico inhalatorio y los glucocorticoides también se encuentran dentro de las opciones, sin haber demostrado un claro beneficio en la evolución del SDRA3, 4. La ventilación con presión positiva sirve para mantener los pacientes con IPA con vida, pero puede contribuir a la progresión de la lesión pulmonar subyacente, causando aumento de la permeabilidad capilar y edema pulmonar. Las altas presiones inspiratorias con grandes volúmenes corrientes llevan a sobredistensión pulmonar y ciclos de apertura y colapso alveolar, todos posibles desencadenantes de lesiones inducidas por el ventilador5 (VILI, Ventilator-Induced Lung Injury).
La estrategia actual de ventilación mecánica convencional en el SDRA es prevenir una lesión
pulmonar secundaria. Ensayos clínicos recientes han demostrado que la limitación de la insuflación pulmonar y la ventilación con medición de las propiedades mecánicas pulmonares se asocian con un mejor resultado. Sin embargo, las técnicas de ventilación con protección pulmonar, utilizando bajo volumen corriente y presión pico de la vía aérea limitada han demostrado una reducción de la mortalidad en pacientes con SDRA3, 6, 7.
La tecnología
Los ECLS pueden proporcionar suficiente intercambio gaseoso en pacientes con IPA, cuando a pesar de la optimización del tratamiento habitual persiste la hipoxemia o la hipercapnia con acidosis respiratoria grave. Esta situación se convierte en una amenaza a la supervivencia del paciente.
La oxigenación por membrana extracorpórea convencional (ECMO, ExtraCorporeal Membrane Oxygenation) se realiza con un oxigenador y una bomba de sangre por fuera del cuerpo a través de cánulas insertas en vías venosas periféricas de gran calibre (yugulares o femorales). Esta técnica requiere de personal específicamente capacitado para manejar un equipo técnico complejo y complicaciones específicas, que se registran entre el 2-6% de los pacientes8.
Se han realizados múltiples esfuerzos para simplificar la utilización y reducir la tasa de complicaciones de los ECLS. Una estrategia ha sido la disminución del tamaño del ECMO, mediante el uso integrado de bombas de sangre rotativas y la optimización de los oxigenadores por membrana capilar a través de la utilización de un compuesto de fibra de polimetilpenteno con el fin de evitar la pérdida de plasma. Esto da como resultado una reducción en los volúmenes de purgado de la bomba y una menor superficie de contacto de la sangre, por lo tanto menores alteraciones en la coagulación (presentes en el 16-32% de los pacientes en ECMO9). Para poder mejorar la seguridad, se ha mejorado la supervisión de la función de la bomba (flujo de sangre, velocidad de rotación, presión arterial y venosa del circuito, estanqueidad, temperatura) y la detección de burbujas10 (mECMO (Figura 1).
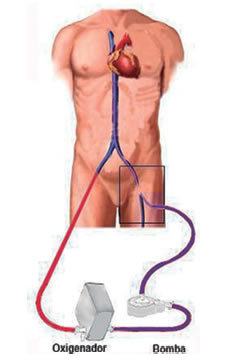
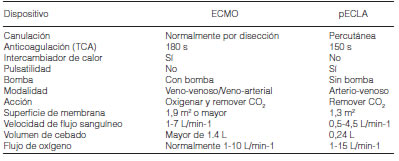
Otra forma de proveer soporte para el intercambio gaseoso es mediante la asistencia pulmonar extracorpórea sin bomba (pECLA, pumpless ExtraCorporeal Lung Support), que integra un oxigenador impulsado por una conexión arteriovenosa sin una bomba de sangre. Usando esta técnica, el gasto cardíaco del paciente es el que conduce la circulación extracorpórea de la sangre; debido a esto es una contraindicación para su uso el bajo gasto cardiaco (GC) y la hipotensión. Estos dispositivos de asistencia pulmonar, Interventional Lung Assist (iLA® Ventilador de membrana, Novalung®11, Hechingen, Alemania), se caracterizan por tener membranas de baja presión y menor superficie extracorpórea, por lo tanto menos contacto con la sangre del paciente. Para el seguimiento de esta técnica, sólo se requiere el control del flujo de sangre extracorpórea, la presión arterial media invasiva y la observación de la perfusión de la extremidad inferior de la arteria canulada. El iLA® es un dispositivo de baja resistencia diseñado para la asistencia respiratoria, con flujo sanguíneo pulsátil a través de membranas de difusión y un revestimiento de matriz de proteínas. Es impulsado por el GC y por lo tanto no requiere la asistencia de la bomba extracorpórea. El sistema iLA® consiste en un sistema de canulación vascular extrapulmonar de un solo uso, completamente montado sobre un sistema de intercambio de gases arteriales y venosos, e incluye un kit de introducción, las cánulas y una membrana de intercambio gaseoso (Figura 2). Este grupo de tecnologías son conocidos como ECCO2R (ExtraCorporeal Carbon Dioxide Removal).
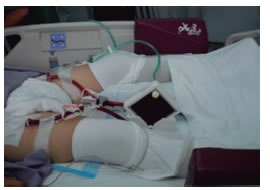
Las diferencias y similitudes de ambas técnicas han sido resumidas en la Tabla 1.
El uso de ECMO para el tratamiento de la IPA grave en adultos, se encuentra autorizado por las agencias de salud de Argentina (ANMAT), EEUU (FDA) y RU (NICE).
Objetivos
Objetivo Primario
Evaluar si disminuye la mortalidad con el uso de dispositivos de ECLS asociados a VM contra el uso de VM solamente, en pacientes adultos con IPA.
Objetivos Secundarios
– Comparar días libres de VM al día 28 entre pacientes con IPA grave tratados con VM sólo vs VM y ECLS combinado.
– Comparar días de internación en el hospital entre pacientes con IPA grave tratados con VM sólo vs VM y ECLS combinado.
– Comparar días de internación en UCI entre pacientes con IPA grave tratados con VM sólo vs VM y ECLS combinado.
- Comparar la respuesta hemodinámica [presión arterial media (TAM) y frecuencia cardiaca (FC)] y los efectos a nivel respiratorio, especialmente la transferencia de gas pulmonar [Presión arterial de dióxido de carbono (PaCO2), Presión arterial de oxígeno (PaO2)] de un ECMOvv contra un pECLA (arterio-venoso) en pacientes agudos con IPA grave.
Evaluar reportes de costo-efectividad del tratamiento con ECLS en IPA.
Contexto
Evaluación desde el contexto hospitalario para definir la incorporación de tecnología y reglamentar su uso.
Población
Pacientes mayores de 17 años de edad, con diagnóstico de IPA grave que requiere altos parámetros de ventilación mecánica para sostener el intercambio gaseoso o que no pueden sostener el mismo a pesar de los altos parámetros.
Intervención
ECLS con VM.
Comparador
VM
Consideraciones
La incorporación de nueva tecnología implica para un hospital un aumento en la calidad de atención a sus pacientes. Existe un grupo de paciente que no responden a la terapia habitual de VM. La no respuesta implica un grupo pequeño de casos. No obstante, la mortalidad de dicho grupo es elevada. Por este motivo, es necesaria la incorporación de nuevas opciones de tratamiento o la planificación de un sistema activo y fluido de derivaciones de dichos casos.
La incorporación de nueva tecnología requiere de un estudio acerca de la evidencia disponible de la misma. Es por ello que llevamos a cabo esta evaluación para definir cuál de las tecnologías disponibles en la actualidad cumple con el mejor balance costo/beneficio entendido tanto en términos de población alcanzada para la intervención y sus ventajas en la mejora de la atención del paciente; así como evaluación de costos actuales del mercado.
Las ventajas de la utilización de pECLA serían una reducción del personal utilizado durante la aplicación de la misma. El uso de ECMOvv requiere la permanencia constante de un técnico perfusionista al lado de la bomba. Mientras que el uso de dispositivos sin bomba puede ser manejado con el mismo personal de la unidad de cuidados intensivo. Los enfermeros con una sencilla capacitación pueden manejar el dispositivo, no así con los sistemas con bomba.
Los centros que efectúen cirugías cardiovasculares con bomba disponen de un circuito de personal y materiales ya en uso con lo cual podrían ampliar el uso del mismo fuera del ámbito del quirófano. No obstante, dada la ocupación de los dispositivos en la terapia, limitarían su potencial uso en el ambiente del quirófano.
Con respecto al espacio físico, es de resaltar el menor tamaño de los dispositivos sin bomba. Con lo cual la utilización de bombas requiere de habitaciones más amplias en superficie para permitir la adecuada circulación del personal.
Teniendo en cuenta estas consideraciones procederemos a evaluar la evidencia de las tecnologías.
Estrategia de búsqueda de información
Trip DataBase
Se efectuó una búsqueda (07/05/2016) en Trip Database con los siguientes términos “(Adult)(Extracorporeal lung assist)(mechanical ventilation) (reduced mortality)”. Se hallaron 66 resultados. Los mismos se discriminan en:
• 3 revisiones sistemáticas (RS),
• 2 sinópticos basados en la evidencia,
• 14 guías de práctica clínica (GPC),
• 2 estudios primarios,
• 2 RS en curso
• 6 ensayos clínicos en curso
• 37 libros de texto
Los últimos se consideraron de bajo nivel de evidencia. Los ensayos clínicos en curso se descartaron por requerir licencia PRO de Trip Database. Las 2 RS en curso se actualizaron al momento de la búsqueda y resultaron en revisiones publicadas por lo que se localizaron. Una fue publicada en Critical Care Canada Forum12 como abstract y fue descartada, mientras que la otra fue publicada en Pubmed13 siendo utilizada para el reporte. Las GPC se descartaron por no responder específicamente la pregunta PICO. Ninguno de sinópticos basados en la evidencia se utilizó por no responder la pregunta PICO. Las RS se descartaron: una de ellas era concerniente a población pediátrica y las otras 2 no respondían adecuadamente la pregunta PICO.
Pubmed
Se efectuó una revisión de publicaciones efectuadas en Pubmed, con la siguiente estrategia de búsqueda:
“Extracorporeal Membrane Oxygenation”[Mesh] AND (pumpless[All Fields] AND extracorporeal[All Fields] AND (“lung”[MeSH Terms] OR “lung”[All Fields]) AND (“helping behavior”[MeSH Terms] OR (“helping”[All Fields] AND “behavior”[All Fields]) OR “helping behavior”[All Fields] OR “assist”[All Fields])) OR (nova[All Fields] AND (“lung”[MeSH Terms] OR “lung”[All Fields])) AND “adult”[MeSH Terms]
Con dicha estrategia se localizaron 209 resúmenes (abstracts). Se localizaron 36 artículos para revisión completa.14-49. Se priorizó la selección de artículos de alta calidad de evidencia (ensayos clínicos aleatorizados [ECCA], RS y GPC).
Se tomaron sólo los trabajos que tuvieron al menos 20 pacientes, ya que la media de las series de casos fue de 19 (1-96). De esa manera, quedaron 12 artículos: 4 ECCA (1 es duplicado) y 8 SC.
Adicionando el filtro de Clinical Queries (Therapy/Broad) e idioma inglés, se reduce a 68 ingresos, pero se pierden algunos estudios importantes. Por ese motivo, lo descartamos.
(Therapy/Broad[filter]) AND (“Extracorporeal Membrane Oxygenation”[Mesh] AND (pumpless[All Fields] AND extracorporeal[All Fields] AND (“lung”[MeSH Terms] OR “lung”[All Fields]) AND (“helping behavior”[MeSH Terms] OR (“helping”[All Fields] AND “behavior”[All Fields]) OR “helping behavior”[All Fields] OR “assist”[All Fields])) OR (nova[All Fields] AND (“lung”[MeSH Terms] OR “lung”[All Fields])) AND “adult”[MeSH Terms)
Se revisaron las citas de los artículos que quedaron para revisión completa y se identificaron 1 ECCA y 3 RS no rescatadas en la búsqueda.
Google
Se efectuó búsqueda en Google de las políticas de cobertura mediante: “extracorporeal lung assist” AND (“coverage policy” OR “coverage policies”). Hallando documentos de Medicare y Blue cross de EEUU50, 51, y del NICE del RU. Se localizaron dos ETS, que incluían una evaluación económica.
Por último mediante búsqueda localizada en los sitios de los sistemas de salud argentino, inglés, canadiense y de los EEUU, se localizaron políticas de cobertura.
Resultados
Estudios primarios
Ensayos clínicos controlados aleatorizados
El ECCA de mayor peso es el protocolo CESAR52. Éste encuentra una reducción de RR a favor del uso de ECMO en pacientes con IPA. El RR de 0,69 IC 95% 0,05-0,97 (p = 0.03) para el grupo ECMO da un dato positivo a favor de su uso. Sin embargo, esta reducción puede ser debida a otros factores. En realidad, todos los pacientes con indicación de ECMO fueron derivados a centros de alta complejidad y volumen. De hecho, sólo el 75% de los pacientes derivados requirieron ECMO. No obstante, parece demostrar beneficios.
Otro ECCA53 que evalúa en este caso a pECLA en combinación con VM protectiva encuentra (en análisis post hoc) aumento significativo de los días libres de VM (a 60 días) de un subgrupo hipoxémico (PaO2/FiO2 < 150) con una mortalidad baja (16,5%); aunque esta última no tiene diferencias significativas. Dichas diferencias no las encontró en el grupo intervención. Concluyen que el uso de pECLA podría tener beneficios en cuanto a las lesiones pulmonares asociadas a ventilador (VILI). Resalta también sus ventajas operativas en el uso.
Otro ECCA54 más antiguo de 1984 evalúa pECLA vs VM convencional sin encontrar diferencias significativas en cuanto a mortalidad a 30 días. Ellos no recomiendan esta estrategia. Cabe recordar que desde el año de este ECCA han cambiado significativamente los dispositivos.
Por último, se reporta un ECCA muy antiguo55 de 1979 realizado en 9 centros de EEUU en pacientes con IPA tratados con ECMOva (n=42) y con VM (N=48). No observaron diferencias en la mortalidad a los 6 meses: ECMO 91% vs VM 92% (RR 0,99 (IC95%: 0,87 a 1,12), ni en la discapacidad posterior. Observaron mayor cantidad de transfusiones en el grupo de pacientes que recibieron ECMO, sin diferencias en la posibilidad de tener un neumotórax (45%) o sepsis (20%).
Estudios observacionales
Las series seleccionadas (Tabla 4), todas con al menos 20 pacientes totalizan 445 pacientes. Son series en su mayoría entre el año 2000 y 2012. Todas son unicétricas siendo 5 de ellas del Hospital Universitario de Regensburg, otra de otro centro de Alemania y la última de un centro de Austria (2015). Es de destacar que el Hospital Universitario de Regensburg fue uno de los promotores de la tecnología pECLA. También descatamos el cambio en la tecnología según los años. A partir de 2009 cambios en las cánulas y bombas de los dispositivos ECMO los hicieron mucho más fáciles de usar. Por ese motivo, vemos el mayor porcentaje de uso de pECLA previo a esa fecha.

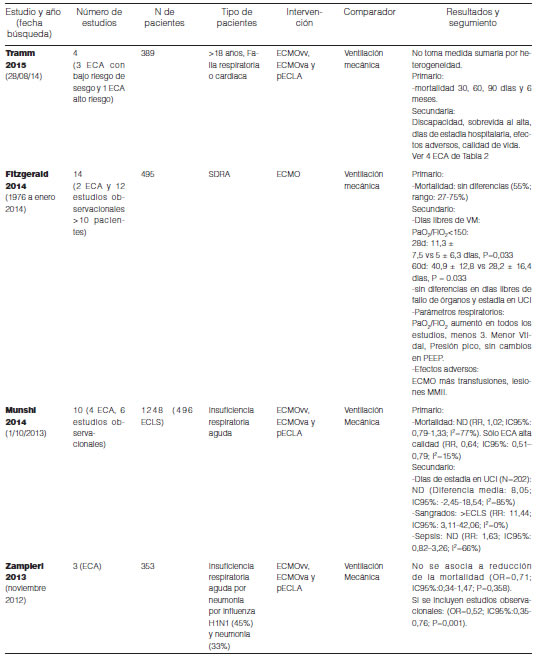
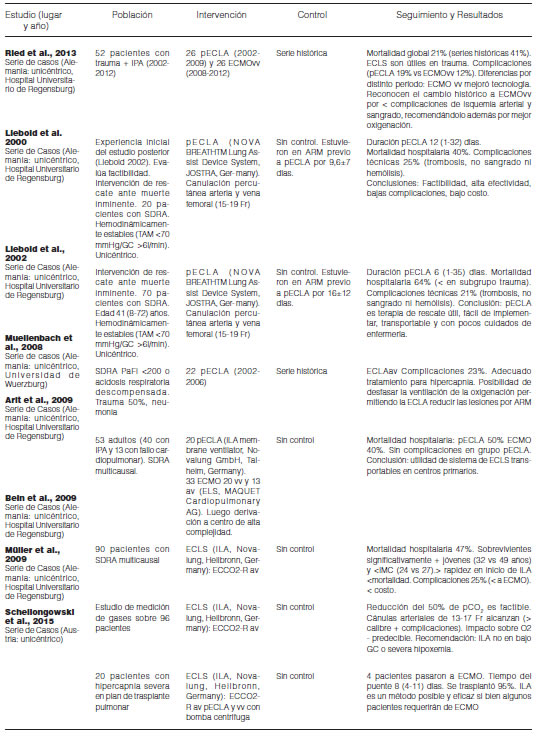
Destacamos en las SC que sólo una descata la reducción de la mortalidad hospitalaria (21% frente a una serie histórica de 40%) con el uso de ECLS este subgrupo es de paciente traumatizados47”container-title”:”Critical Care (London, England. Este mismo grupo (en otro trabajo) descata el mejor pronóstico de los pacientes más jóvenes y con un IMC menor.
En general, los trabajos resaltan la facilidad y rapidez en el uso de pECLA pero advierten que los beneficios de pECLA están dados en mejora de la acidosis y la hipercapnia solamente; sin observar beneficios en la oxigenación. Recomiendan (la mayor parte de las series) el uso de ECMOvv por menores complicaciones sobre todo luego del 2008.
Estudios secundarios
Revisiones sistemáticas
Fitzgerald et al13”container-title”:”Critical Care”, ”page”:”222”,”volume”:”18”,”issue”:”3,”source”: ”PubMed Central”,”abstract”:”Acute respiratory distress syndrome (ARDS evalúan los dispositivos de remoción de CO2 en pacientes con IPA causada por SDRA en comparación a VM. Estos requieren o canulación arterio- venosa o veno-venosa. No obstante, ambos no utilizan bomba. Es por eso que su principal función radica en la remoción del CO2 y no en la oxigenación propiamente dicha. Incluyeron en la revisión 2 ECCA y 12 SC con 10 o más pacientes, contabilizando un total de 495 pacientes en la RS. Encuentran que no hay diferencias en cuanto a la mortalidad y días de internación en UTI de los grupos. No obstante, en un análisis post hoc encuentran disminución de los días de VM. Destacan la eficacia de estos dispositivos en remover CO2 aunque advierten la falta de ECCA adecuados para evaluar diferencias en la mortalidad.
Tramm et al56”container-title”:”Cochrane Database of Systematic Reviews”,”publisher”:”John Wiley & Sons, Ltd”,”source”:”Wiley Online Library”,”abstract”:”Background\nBackground\n\ nExtracorporeal membrane oxygenation (ECMO evalúan ECMO en sus dos modalidades (av y vv) en comparación a la VM tradicional. Incluyen 4 ECCA que representan 389 pacientes con IPA con una calidad de evidencia entre baja y moderada. Informan la falta de diferencias significativas en cuanto a mortalidad a 30 días y a 6 meses. Tampoco encuentra diferencias en cuando a discapacidad a 6 meses. Concluyen que ECMO sigue siendo una terapia de rescate.
Munshi et al57 evaluaron ECMOvv, ECMOva y pECLA en comparación a VM convencional hasta el 01/10/2013. Incluyen 10 estudios (4 ECCA, 6 estudios observacionales) que representan 1.248 (496 ECLS) pacientes con IPA. Evalúan como resultado primario la mortalidad sin encontrar diferencias (RR, 1,02; IC95%: 0,79–1,33; I2=77%), sólo pudieron encontrar disminución de la mortalidad con el uso de ECLS en dispositivos veno-venosos y sólo en estudios randomizados o cuasi-randomizados (RR, 0,64; IC95%: 0,51-0,79; I2=15%). Dentro de los resultados secundarios, evaluaron la estadía en UCI (N=202) sin encontrar diferencias entre el uso de ECLS y VM (diferencia media: 8,05; IC95%: -2,45-18,54; I2=85%). Sí observaron un incremento en los sangrados con el uso de ECLS (RR: 11,44; IC95%: 3,11–42,06; I2=0%), sin diferencias en el riesgo de sufrir sepsis (RR: 1,63; IC95%: 0,82–3,26; I2=66%).
Zampieri et al58 incluyeron tres estudios en el metanálisis, comprendiendo 353 pacientes en el análisis principal, de los cuales 179 pacientes fueron tratados con ECLS. Un estudio era un ECCA y dos eran estudios observacionales. La causa más común de IPA fue neumonía por influenza H1N1 (45%) y neumonía (33%). El uso de ECLS no se asoció con una reducción de la mortalidad hospitalaria (OR=0,71; IC95%= 0,34-1,47; P=0,358). Con los dos estudios observacionales se incluyeron un total de 478 casos, en los cuales 228 recibieron apoyo con ECLS. En el primer análisis, el uso de ECLS tuvo una disminución de la mortalidad hospitalaria (OR=0,52; IC95 %= 0,35-0,76; P=0,001).
Evaluaciones económicas
Los pacientes asignados a ECMO incurren en promedio en un costo total de £73.979 en comparación con £33.435 para los que se someten a VM solamete (precios del RU, 2005). En el seguimiento luego de 6 meses de la asignación al azar, el costo adicional de un sobreviviente y sin discapacidad grave de ECMO en comparación con VM fue de £251.360. El tratamiento con ECMO dio lugar a 0,03 QALYs adicionales a los predichos, a los 6 meses de seguimiento. Un modelo de sobrevida predijo un costo por QALYs de la ECMO de £19.252 (IC95% £7.622 a £59.200) con una tasa de descuento de 3,5 %. Los QALYs ganados fueron 10,75 para el grupo de ECMO en comparación con 7,31 para el grupo convencional52.
Otro reporte efectúa una evaluación de costos y costo-efectividad comparando ECMO con VM. Describen en la literatura un riesgo de sesgo bajo y una fortaleza de evidencia baja. Concluyen en la costo-efectividad del ECMO con un costo de USD 7.000-35.000 por QALY ganado, con un costo incremental entre USD 100.000-500.000 para EEUU50.
Evaluaciones de Tecnologías Sanitarias
Se encontró una ETS50 realizada por el Institute for Clinical and Economic Review59. La misma fue realizada para The Washington State Health Care Authority60, la que otorga salud para de ciudadanos de Washington, EEUU (incluye Medicaid61 y empleados públicos). Esta ETS evalúa ECMO y dispositivos pECLA (pECLA, ECCO2Rav e iLA®) en todas sus indicaciones en general: como apoyo cardíaco, apoyo pulmonar, puente al trasplante cardiopulmonar y dispositivo de reanimación cardiopulmonar extracorpóreo. Nos abocaremos al apoyo pulmonar que es el objetivo de la presente. Reportan con respecto a este último uso: 2 ECCA y 5 estudios de cohorte, representando 691 pacientes. Describen en la literatura un nivel de sesgo medio y fortaleza de evidencia moderada. Encuentran al ECMO comparable a ARM sin hallar diferencias en cuanto a supervivencia, tiempo de estadía y discapacidad posterior.
Concluyen que la tecnología ECMO es comparable a ARM aunque puede llegar a ser mejor.
Políticas de cobertura
Argentina
Específicamente se realizó una búsqueda en línea dirigida en ANMAT. Se detallan las indicaciones aprobadas para ECMO62 y para Novalung63 como representante de pECLA:
1. ECMO como reemplazo pulmonar es entendido como terapia de sustitución.
2. Novalung® está autorizado como un sistema respiratorio con protección pulmonar en situaciones en las que no se observe un intercambio gaseoso suficiente, en especial en cuanto a la eliminación de CO2 (ejemplos: SDRA o IPA de causa pulmonar o extrapulmonar, EPOC exacerbada, solución provisional previa al trasplante pulmonar, ventilación protectiva con elevada presión intracraneal, fístulas broncopleurales).
3. También se indica para situaciones clínicas en las que el pacientes requiera gran esfuerzo para mantener la ventilación espontánea o se tema colapso de la bomba respiratoria: EPOC exacerbada, destete complicado.
Reino Unido
Se encontraron políticas de coberturas de NICE para ECMO64 y para dispositivos de remoción de CO2 extracorpóreos65. Para ECMO detallan que es una terapia de soporte para adultos con IPA severa de causa potencialmente reversible. Hacen una aclaración en cuanto a los removedores veno-venosos con bomba de CO2 sanguíneo: han sido recientemente introducidos como terapeútica y no hay evidencia sustancial publicada sobre esta técnica. Con respecto al resto de los dispositivos de remoción de CO2, lo indican en fallo respiratorio hipercápnico o puente al trasplante y SDRA. Aclaran que el tratamiento convencional de la IPA severa es la VM. Sin embargo, en algunos pacientes no se logra un adecuado intercambio gaseoso a pesar de usar las máximas presiones que el pulmón puede tolerar.
EEUU
Se encontraron políticas de cobertura para ECMO similares en compañías de salud privadas de EEUU66 como en Medicare y Medicaid67, 68 y diferentes estados51, 69.
Entre las situaciones clínicas en las que está indicado y cubierto el inicio de ECMO se incluyen las siguientes:
1. insuficiencia respiratoria hipoxémica con una PaO2/FiO2 < 100 mmHg a pesar de la optimización de los parámetros del ventilador, incluyendo el volumen corriente, la presión positiva al final de la espiración (PEEP) y la relación inspiratoria/espiratoria (I:E),
2. insuficiencia respiratoria hipercápnica con un pH arterial de menos de 7,20,
3. shock cardiogénico refractario,
4. la falta de desconexión de un bypass cardiopulmonar después de la cirugía cardiaca,
5. Como un puente para el trasplante cardíaco, ya sea o la colocación de un dispositivo de asistencia ventricular.
Se encuentra contraindicado en casos que esté contraindicada la anticoagulación, cuando el paciente se encuentra ventilado hace más de 7 días, entre otras.
Conclusiones
La evidencia actual del uso de ECMO en la IPA demuestra reducción de la mortalidad en el corto tiempo (30 días o intrahospitalaria) en comparación con VM. No se encontraron diferencias a largo plazo. Tampoco se encontraron diferencias en los días libres de VM al día 28, en la estadía hospitalaria, ni en la estadía en UCI.
Con respecto al uso de los dispositivos, en pECLA la evidencia es de menor calidad y si bien muestran un futuro promisorio, no hay evidencia de reducción de mortalidad con su uso.
Los parámetros hemodinámicos no son modificados por el ECMOvv ni por los pECLA. De hecho, es necesaria la estabilidad hemodinámica para su uso. El ECMOav es en los casos de inestabilidad hemodinámica.
En relación a la transferencia de gas pulmonar observamos que la mayoría de los trabajos publicados coinciden en la mejoría (reducción de la PaCO2 y aumento de la PaO2) con el uso de ECLS. El mayor beneficio se encuentra en el tratamiento de la hipercapnia, para la cual los pECLA parecen ser los más indicados, en relación a su menor complejidad y costo. Es de resaltar que muchas publicaciones coinciden en tasas menores de complicaciones con el uso de pECLA con respecto a ECMOvv, en particular con respecto a la coagulación y hemólisis.
El uso de ECMO y pECLA están autorizados en Argentina, Reino Unido y EEUU, y en la mayoría de los países europeos. Las indicaciones deben ser estrictamente controladas y monitorizadas. Los sistemas de salud hacen especial hincapié en la derivación a centros de alto volumen y complejidad para su uso.
Con respecto a los costos, encontramos costo efectividad para ECMO en los sistemas de salud de EEUU y el RU, con valores de USD 7.000-35.000 por año de vida o QALY ganado y de £19.252 (IC95% 7.622-59.200) para pECLA.
Un reporte habla del menor costo del uso de pECLA con respecto a ECMO con una relación de 5 a 1 a favor de los pECLA. No obstante, dado que su superioridad no está demostrada, no parece relevante.
Conflicto de interés: Los autores del trabajo declaran no tener conflictos de intereses relacionados con esta publicación.
1. Mercat A, Richard J-CM, Vielle B, Jaber S, Osman D, Diehl J-L, et al. Positive end-expiratory pressure setting in adults with acute lung injury and acute respiratory distress syndrome: a randomized controlled trial. JAMA. 2008 Feb 13; 299(6): 646-55.
2. ARDS Definition Task Force, Ranieri VM, Rubenfeld GD, Thompson BT, Ferguson ND, Caldwell E, et al. Acute respiratory distress syndrome: the Berlin Definition. JAMA. 2012 Jun 20; 307(23): 2526-33.
3. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. The Acute Respiratory Distress Syndrome Network. N Engl J Med. 2000 May 4; 342(18): 1301-8.
4. Girard TD, Bernard GR. Mechanical ventilation in ARDS: a state-of-the-art review. Chest. 2007 Mar; 131(3): 921-9.
5. de Prost N, Ricard J-D, Saumon G, Dreyfuss D. Ventilator-induced lung injury: historical perspectives and clinical implications. Ann Intensive Care. 2011 Jul 23; 1: 28.
6. Amato MB, Barbas CS, Medeiros DM, Magaldi RB, Schettino GP, Lorenzi-Filho G, et al. Effect of a protective-ventilation strategy on mortality in the acute respiratory distress syndrome. N Engl J Med. 1998 Feb 5; 338(6): 347-54.
7. Ware LB, Matthay MA. The acute respiratory distress syndrome. N Engl J Med. 2000 May 4; 342(18): 1334-49.
8. Mols G, Loop T, Geiger K, Farthmann E, Benzing A. Extracorporeal membrane oxygenation: a ten-year experience. Am J Surg. 2000 Aug; 180 (2): 144-54.
9. Conrad SA, Rycus PT, Dalton H. Extracorporeal Life Support Registry Report 2004. ASAIO J Am Soc Artif Intern Organs 1992. 2005 Feb; 51(1): 4-10.
10. Kopp R, Bensberg R, Wardeh M, Rossaint R, Kuhlen R, Henzler D. Pumpless arterio-venous extracorporeal lung assist compared with veno-venous extracorporeal membrane oxygenation during experimental lung injury. Br J Anaesth. 2012 May; 108(5): 745-53.
11. Novalung. Solutions for lung failure. [Internet]. [cited 2016 May 19]. Available from: http://www.novalung.com/en/home
12. Tillmann B, Klingel M, Iansavitchene A, Nagpal D. Extracorporeal membrane oxygenation (ECMO) as a treatment strategy for severe acute respiratory distress syndrome (ARDS) in the low tidal volume era: a systematic review. Crit Care Can Forum [Internet]. 2014 [cited 2016 May 8]; Available from:
http://www.criticalcarecanada.com/abstracts/2014/extracorporeal_membrane_oxygenation_as_a_
treatment_strategy_for_severe_acute_respiratory_distress_syndrome_in_the_low_
tidal_volume_era_a_systematic_review.php
13. Fitzgerald M, Millar J, Blackwood B, Davies A, Brett SJ, McAuley DF, et al. Extracorporeal carbon dioxide removal for patients with acute respiratory failure secondary to the acute respiratory distress syndrome: a systematic review. Crit Care. 2014; 18(3): 222.
14. Liebold A, Reng CM, Philipp A, Pfeifer M, Birnbaum DE. Pumpless extracorporeal lung assist - experience with the first 20 cases. Eur J Cardio-Thorac Surg Off J Eur Assoc Cardio-Thorac Surg. 2000 May; 17(5): 608-13.
15. Liebold A, Philipp A, Kaiser M, Merk J, Schmid FX, Birnbaum DE. Pumpless extracorporeal lung assist using an arterio-venous shunt. Applications and limitations. Minerva Anestesiol. 2002 May; 68(5): 387-91.
16. Reng M, Philipp A, Kaiser M, Pfeifer M, Gruene S, Schoelmerich J. Pumpless extracorporeal lung assist and adult respiratory distress syndrome. Lancet Lond Engl. 2000 Jul 15; 356(9225): 219-20.
17. Möller JC, Schaible TF, Ahrens W, Kohl M. Pumpless extracorporeal lung assist. Lancet Lond Engl. 2000 Sep 23; 356(9235): 1112.
18. Zimmermann M, Bein T, Philipp A, Ittner K, Foltan M, Drescher J, et al. Interhospital transportation of patients with severe lung failure on pumpless extracorporeal lung assist. Br J Anaesth. 2006 Jan; 96(1): 63-6.
19. Bein T, Weber F, Philipp A, Prasser C, Pfeifer M, Schmid F-X, et al. A new pumpless extracorporeal interventional lung assist in critical hypoxemia/hypercapnia. Crit Care Med. 2006 May; 34(5): 1372-7.
20. von Mach M-A, Kaes J, Omogbehin B, Sagoschen I, Wiechelt J, Kaiser K, et al. An update on interventional lung assist devices and their role in acute respiratory distress syndrome. Lung. 2006 Jun; 184(3): 169-75.
21. Mallick A, Elliot S, McKinlay J, Bodenham A. Extracorporeal carbon dioxide removal using the Novalung in a patient with intracranial bleeding. Anaesthesia. 2007 Jan; 62(1): 72-4.
22. Zimmermann M, Philipp A, Schmid F-X, Dorlac W, Arlt M, Bein T. From Baghdad to Germany: use of a new pumpless extracorporeal lung assist system in two severely injured US soldiers. ASAIO J Am Soc Artif Intern Organs 1992. 2007 Jun; 53(3) :e4-6.
23. Jouvet P, Farges C, Hatzakis G, Monir A, Lesage F, Dupic L, et al. Weaning children from mechanical ventilation with a computer-driven system (closed-loop protocol): a pilot study. Pediatr Crit Care Med J Soc Crit Care Med World Fed Pediatr Intensive Crit Care Soc. 2007 Sep; 8(5): 425-32.
24. Iglesias M, Martinez E, Badia JR, Macchiarini P. Extrapulmonary ventilation for unresponsive severe acute respiratory distress syndrome after pulmonary resection. Ann Thorac Surg. 2008 Jan; 85(1): 237-44; discussion 244.
25. Muellenbach RM, Kredel M, Wunder C, Küstermann J, Wurmb T, Schwemmer U, et al. Arteriovenous extracorporeal lung assist as integral part of a multimodal treatment concept: a retrospective analysis of 22 patients with ARDS refractory to standard care. Eur J Anaesthesiol. 2008 Nov; 25(11): 897-904.
26. Hommel M, Deja M, von Dossow V, Diemel K, Heidenhain C, Spies C, et al. Bronchial fistulae in ARDS patients: management with an extracorporeal lung assist device. Eur Respir J. 2008 Dec; 32(6): 1652-5.
27. Bein T, Zimmermann M, Hergeth K, Ramming M, Rupprecht L, Schlitt HJ, et al. Pumpless extracorporeal removal of carbon dioxide combined with ventilation using low tidal volume and high positive end-expiratory pressure in a patient with severe acute respiratory distress syndrome. Anaesthesia. 2009 Feb; 64(2): 195-8.
28. Pesenti A, Zanella A, Patroniti N. Extracorporeal gas exchange. Curr Opin Crit Care. 2009 Feb; 15(1): 52-8.
29. Arlt M, Philipp A, Zimmermann M, Voelkel S, Amann M, Bein T, et al. Emergency use of extracorporeal membrane oxygenation in cardiopulmonary failure. 2. 2009 Sep; 33(9): 696-703.
30. Fernández P, Muñoz P, Fischer D, Méndez F, Florenzano M, Valdés S, et al. [Bridge to lung transplantation with a novel pumpless lung assist device. Report of one case]. Rev Médica Chile. 2009 Oct; 137(10): 1363-6.
31. Freed DH, Henzler D, White CW, Fowler R, Zarychanski R, Hutchison J, et al. Extracorporeal lung support for patients who had severe respiratory failure secondary to influenza A (H1N1) 2009 infection in Canada. Can J Anaesth J Can Anesth. 2010 Mar; 57(3): 240-7.
32. Floerchinger B, Philipp A, Foltan M, Rupprecht L, Klose A, Camboni D, et al. Switch from venoarterial extracorporeal membrane oxygenation to arteriovenous pumpless extracorporeal lung assist. Ann Thorac Surg. 2010 Jan; 89(1): 125-31.
33. Aniset L, Kalenka A. [Status asthmaticus. Role of extracorporeal lung assist procedures]. Anaesthesist. 2010 Apr; 59(4): 327-32.
34. Litmathe J, Dapunt O. Double ECMO in severe ARDS: report of an outstanding case and literature review. Perfusion. 2010 Nov; 25(6): 363-7.
35. Jung C, Lauten A, Pfeifer R, Bahrmann P, Figulla HR, Ferrari M. Pumpless extracorporeal lung assist for the treatment of severe, refractory status asthmaticus. 2. 2011 Feb; 48(1): 111-3.
36. Haneya A, Philipp A, Mueller T, Lubnow M, Pfeifer M, Zink W, et al. Extracorporeal circulatory systems as a bridge to lung transplantation at remote transplant centers. Ann Thorac Surg. 2011 Jan; 91(1): 250-5.
37. Lange J, Knüttgen D, Stoelben E, Bauerfeind U, Wappler F, Sakka SG. [Interventional lung assist membrane ventilator. Successful use despite heparin-induced thrombocytopenia type II]. Anaesthesist. 2011 Mar; 60(3): 230-5.
38. Lange J, Heiss M, Wappler F, Sakka SG. Unexpected effects on arterial oxygenation during reduction in oxygen flow via a pumpless lung assist system. Minerva Anestesiol. 2011 Mar; 77(3): 375-7.
39. Banach M, Soukup J, Bucher M, Andres J. High frequency oscillation, extracorporeal membrane oxygenation and pumpless arteriovenous lung assist in the management of severe ARDS. Anestezjol Intensywna Ter. 2010 Dec; 42(4): 201-5.
40. Wilbring M, Petzoldt M, Gulbins H, Goetz AE, Reichenspurner H. Successful weaning from extracorporal circulation using a pumpless extracorporal lung assist device in a patient with intraoperative hypercapnic lung failure during aortic valve replacement. Thorac Cardiovasc Surg. 2012 Jun; 60(4): 299-301.
41. Bartosik W, Egan JJ, Wood AE. The Novalung interventional lung assist as bridge to lung transplantation for self-ventilating patients - initial experience. 2. 2011 Aug; 13(2): 198-200.
42. Johnson P, Fröhlich S, Westbrook A. Use of extracorporeal membrane lung assist device (Novalung) in H1N1 patients. J Card Surg. 2011 Jul; 26(4): 449-52.
43. Nierhaus A, Frings D, Braune S, Baumann H-J, Schneider C, Wittenburg B, et al. Interventional lung assist enables lung protective mechanical ventilation in acute respiratory distress syndrome. Minerva Anestesiol. 2011 Aug; 77(8): 797-801.
44. Petzoldt M, Braune S, Bittmann I, Kluge S. Rescue therapy with a pumpless extracorporeal lung assist device in a patient with acute interstitial lung disease and severe refractory hypercapnia. Respir Care. 2012 Feb; 57(2): 293-7.
45. Cordier P-Y, Nau A, Peytel E. [Acute respiratory distress syndrome treated by pumpless extracorporeal lung assist device]. Ann Fr Anesthèsie Rèanimation. 2011 Dec; 30(12): 937-8.
46. Coscia AP, Cunha HFR da, Longo AG, Martins EGS, Saddy F, Japiassu AM. Report of two cases of ARDS patients treated with pumpless extracorporeal interventional lung assist. J Bras Pneumol Publicação Of Soc Bras Pneumol E Tisilogia. 2012 Jun; 38(3): 408-11.
47. Ried M, Bein T, Philipp A, Müller T, Graf B, Schmid C, et al. Extracorporeal lung support in trauma patients with severe chest injury and acute lung failure: a 10-year institutional experience. Crit Care Lond Engl. 2013; 17(3): R110.
48. Schellongowski P, Riss K, Staudinger T, Ullrich R, Krenn CG, Sitzwohl C, et al. Extracorporeal CO2 removal as bridge to lung transplantation in life-threatening hypercapnia. Transpl Int Off J Eur Soc Organ Transplant. 2015 Mar; 28(3): 297-304.
49. Redwan B, Semik M, Dickgreber N, Ziegeler S, Fischer S. Single site cannulation veno-venous extracorporeal lung support during pulmonary resection in patients with severely compromised pulmonary function. ASAIO J Am Soc Artif Intern Organs 1992. 2015 Jun; 61(3): 366-9.
50. Travers K, Russo E, Synnott P, Chapman R, Pearson S, Ollendorf D. Extracorporeal Membrane Oxygenation (ECMO) [Internet]. Institute for Clinical and Economic Review (ICER); 2015 Dec [cited 2016 May 8]. (Health Technology Assessment Program). Available from: http://www.hca.wa.gov/hta/Documents/ecmo_draft_report_121115.pdf
51. HMSA (Blue Cross). Extracorporeal Membrane Oxygenation (ECMO). Policy Number: Original Effective Date:MM.12.006 05/16/2006. [Internet]. [cited 2016 May 19]. Available from:
http://www.hmsa.com/PORTAL/PROVIDER/MM.12.006_Extracorporeal_Membrane_Oxygenation_(ECMO)_110114.pdf
52. Peek GJ, Mugford M, Tiruvoipati R, Wilson A, Allen E, Thalanany MM, et al. Efficacy and economic assessment of conventional ventilatory support versus extracorporeal membrane oxygenation for severe adult respiratory failure (CESAR): a multicentre randomised controlled trial. The Lancet. 2009 Oct; 374(9698): 1351-63.
53. Bein T, Weber-Carstens S, Goldmann A, Müller T, Staudinger T, Brederlau J, et al. Lower tidal volume strategy (≈3 ml/kg) combined with extracorporeal CO2 removal versus “conventional” protective ventilation (6 ml/kg) in severe ARDS. Intensive Care Med. 2013 May; 39(5): 847-56.
54. Morris AH, Wallace CJ, Menlove RL, Clemmer TP, Orme JF, Weaver LK, et al. Randomized clinical trial of pressure-controlled inverse ratio ventilation and extracorporeal CO2 removal for adult respiratory distress syndrome. Am J Respir Crit Care Med. 1994 Feb; 149(2 Pt 1): 295-305.
55. Zapol WM, Snider MT, Hill JD, Fallat RJ, Bartlett RH, Edmunds LH, et al. Extracorporeal membrane oxygenation in severe acute respiratory failure. A randomized prospective study. JAMA. 1979 Nov 16; 242(20): 2193-6.
56. Tramm R, Ilic D, Davies AR, Pellegrino VA, Romero L, Hodgson C. Extracorporeal membrane oxygenation for critically ill adults. In: Cochrane Database of Systematic Reviews [Internet]. John Wiley & Sons, Ltd; 2015 [cited 2016 May 8]. Available from: http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD010381.pub2/abstract
57. Munshi L, Telesnicki T, Walkey A, Fan E. Extracorporeal life support for acute respiratory failure. A systematic review and metaanalysis. Ann Am Thorac Soc. 2014 Jun; 11(5): 802-10.
58. Zampieri FG, Mendes PV, Ranzani OT, Taniguchi LU, Pontes Azevedo LC, Vieira Costa EL, et al. Extracorporeal membrane oxygenation for severe respiratory failure in adult patients: a systematic review and meta-analysis of current evidence. J Crit Care. 2013 Dec; 28(6): 998-1005.
59. ICER - ICER is a trusted non-profit organization that evaluates evidence on the value of medical tests, treatments and delivery system innovations and moves that evidence into action to improve the health care system. [Internet]. [cited 2016 May 19]. Available from: http://icer-review.org/
60. Health Care Authority [Internet]. [cited 2016 May 19]. Available from: http://www.hca.wa.gov/Pages/index.aspx
61. Medicaid Home [Internet]. [cited 2016 May 19]. Available from: https://www.medicaid.gov/
62. ECMO ANMAT [Internet]. [cited 2016 May 10]. Available from:
http://www.anmat.gov.ar/boletin_anmat/agosto_2013/Dispo_5473-13.pdf
63. Novalung ANMAT [Internet]. [cited 2016 May 10]. Available from: http://www.anmat.gov.ar/boletin_anmat/enero_2016/Dispo_0789-16.pdf
64. Extracorporeal membrane oxygenation for severe acute respiratory failure in adults | Guidance and guidelines | NICE [Internet]. [cited 2016 Jun 14]. Available from:https://www.nice.org.uk/guidance/ipg
65. Extracorporeal membrane carbon dioxide removal | Guidance and guidelines | NICE [Internet]. [cited 2016 Jun 14]. Available from: https://www.nice.org.uk/guidance/ipg428
66. Premera Blue Cross. Extracorporeal Membrane Oxygenation for Adult Conditions [Internet]. [cited 2016 May 19]. Available from: https://www.premera.com/medicalpolicies/8.01.60.pdf
67. Medicare C for, Baltimore MS 7500 SB, Usa M. RVU15A [Internet]. 2014 [cited 2016 May 19]. Available from: https://www.cms.gov/Medicare/Medicare-Fee-for-Service-Payment/PhysicianFeeSched/PFS-Relative- Value-Files-Items/RVU15A.html?DLPage=1&DLSort=0&DLSortDir=descending
68. Blue Cross Blue Shield of Arizona. Extracorporeal membrane oxygenation (ECMO) for adult respiratory failure [Internet]. [cited 2016 May 19]. Available from: https://www.azblue.com/~/media/azblue/files/healthcare/resources/medical-coverage-guidelines/medicine/o951.pdf
69. Regence of Oregon and Utah. Extracorporeal Membrane Oxygenation (ECMO) for the Treatment of Cardiac and Respiratory Failure in Adults [Internet]. [cited 2016 May 19]. Available from: http://blue.regence.com/trgmedpol/medicine/med152.pdf